近日,我院应光国教授团队抗生素耐药性研究小组白红、何良英、高方舟等人在环境与生态领域期刊Environment International上发表了题为“Airborne antibiotic resistome and microbiome in pharmaceutical factories”的研究性文章

图文摘要
全文速览
本研究通过宏基因组测序对三家大型抗生素制药厂不同功能区(厂区、污水处理区和居民区)的空气抗生素抗性组和微生物组进行了系统分析。研究显示,制药厂空气中含有多种临床重要抗生素抗性基因(ARGs)(vanR/vanS、blaOXA和CfxA)。污水处理区相较于厂区及居民区,其气载ARGs的相对丰度更高(0.64 copies/16S rRNA)。在检测到的所有气载ARGs中,约有28.2%的ARGs被质粒序列携带,而在污水处理区这一比例上升至约50%。贝叶斯溯源分析显示制药厂内土壤和污水处理区废水是气载ARGs的主要来源。此外,1,043个病毒操作分类单元(vOTU)及应对噬菌体感染的不同CRISPR-Cas系统在制药厂空气中被注释。最后本研究根据ARGs可移动性及潜在病原菌宿主,提供了一份制药厂气载高风险ARGs清单。本研究通过对三家大型制药厂空气的宏基因组分析,解析了制药厂气载抗生素抗性组和微生物组的分布特征,揭示了ARGs通过质粒及噬菌体的潜在传播途径,提供了制药厂气载高风险ARGs清单。
引言
抗生素耐药性是全球公共健康领域的重大挑战,而空气传播是ARGs在环境传播中一个重要但却未得到足够重视的途径。自抗生素广泛使用以来,抗生素活性药物成分(API)和制剂的产量大幅增加。以往的研究表明,抗生素制药厂是周围受纳水体和土壤环境中ARGs和耐药菌(ARB)的主要来源,但其在空气中的传播规律及其环境风险仍知之甚少。本研究结果有助于对遏制细菌耐药性蔓延提供科学依据,并提高人们对空气生物安全的意识。
图文导读
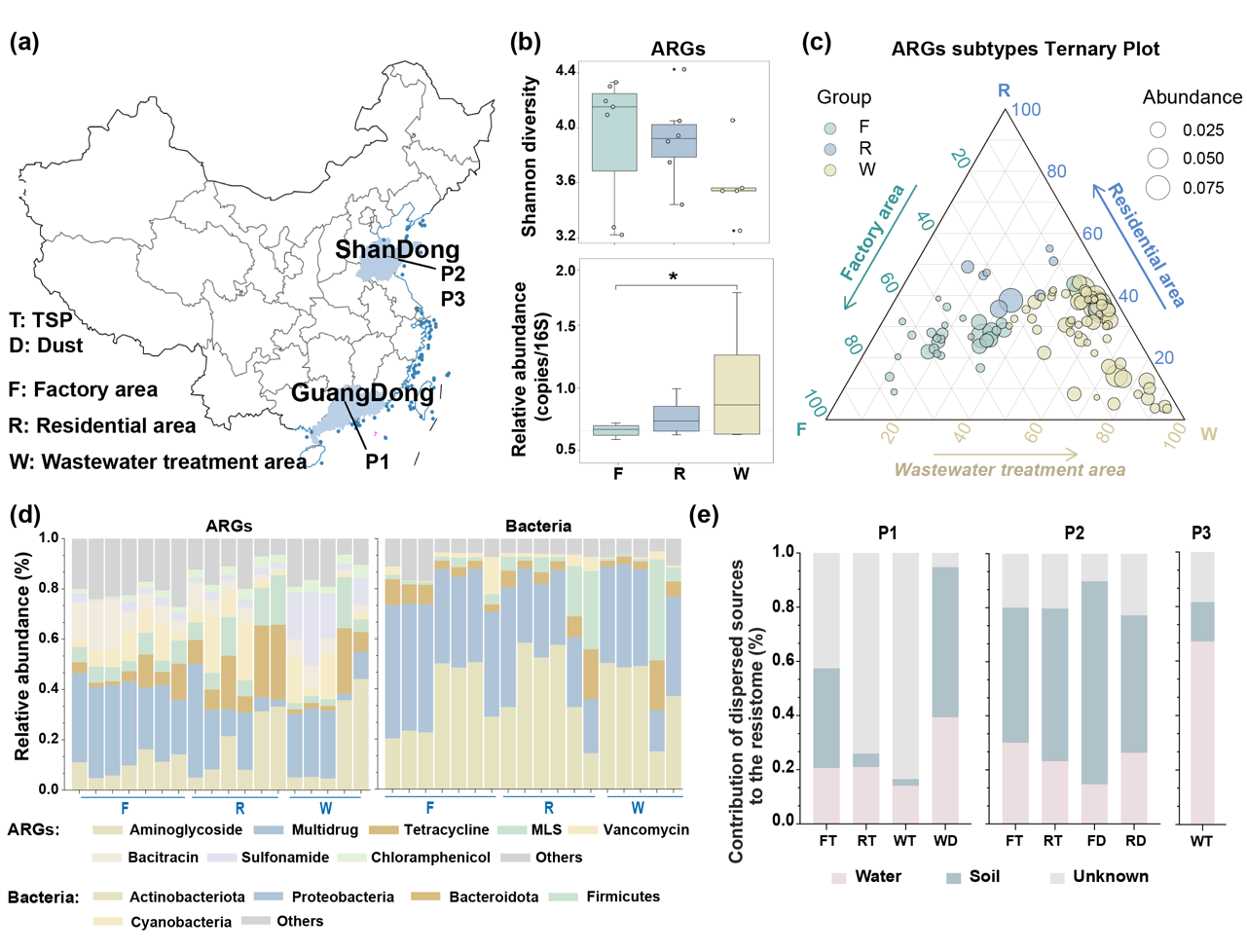
Figure 1. Profiles of airborne resistome and microbiome at pharmaceutical factories.
制药厂气载ARGs主要类别为氨基糖苷类和四环素类,气载细菌的主要类别为放线菌门和变形菌门。不同功能区气载ARGs分析显示,污水处理区显示出更高丰度的气载ARG。利用贝叶斯溯源分析表明,16.53-94.75%的气载ARGs来自制药厂土壤(14.10-67.24%)和污水处理区废水(2.43-75.06%),表明制药厂内各种环境介质抗性基因之间存在潜在的相互作用。
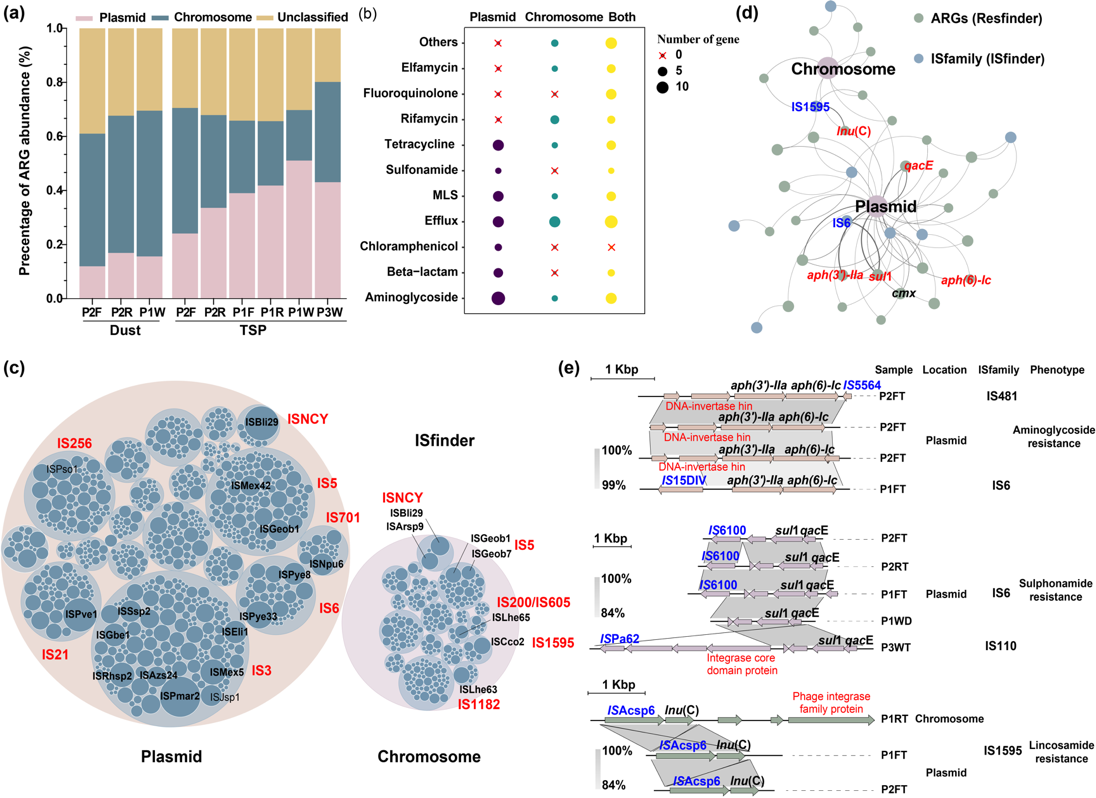
Figure 2. Profiles of airborne ARGs mobility potential.
本研究在制药厂空气中识别到28.20%的ARGs定位在质粒上(414/1468),40.53%位于染色体(595/1468)。通过对插入序列(IS)的注释显示,与染色体相比质粒上携带的IS丰度更高。IS3,IS5和IS236家族是质粒上常见的IS类型,而与ARGs共定位频繁的IS类型为IS6家族。此外,噬菌体整合酶蛋白也可能参与ARGs在染色体和质粒之间潜在转移。
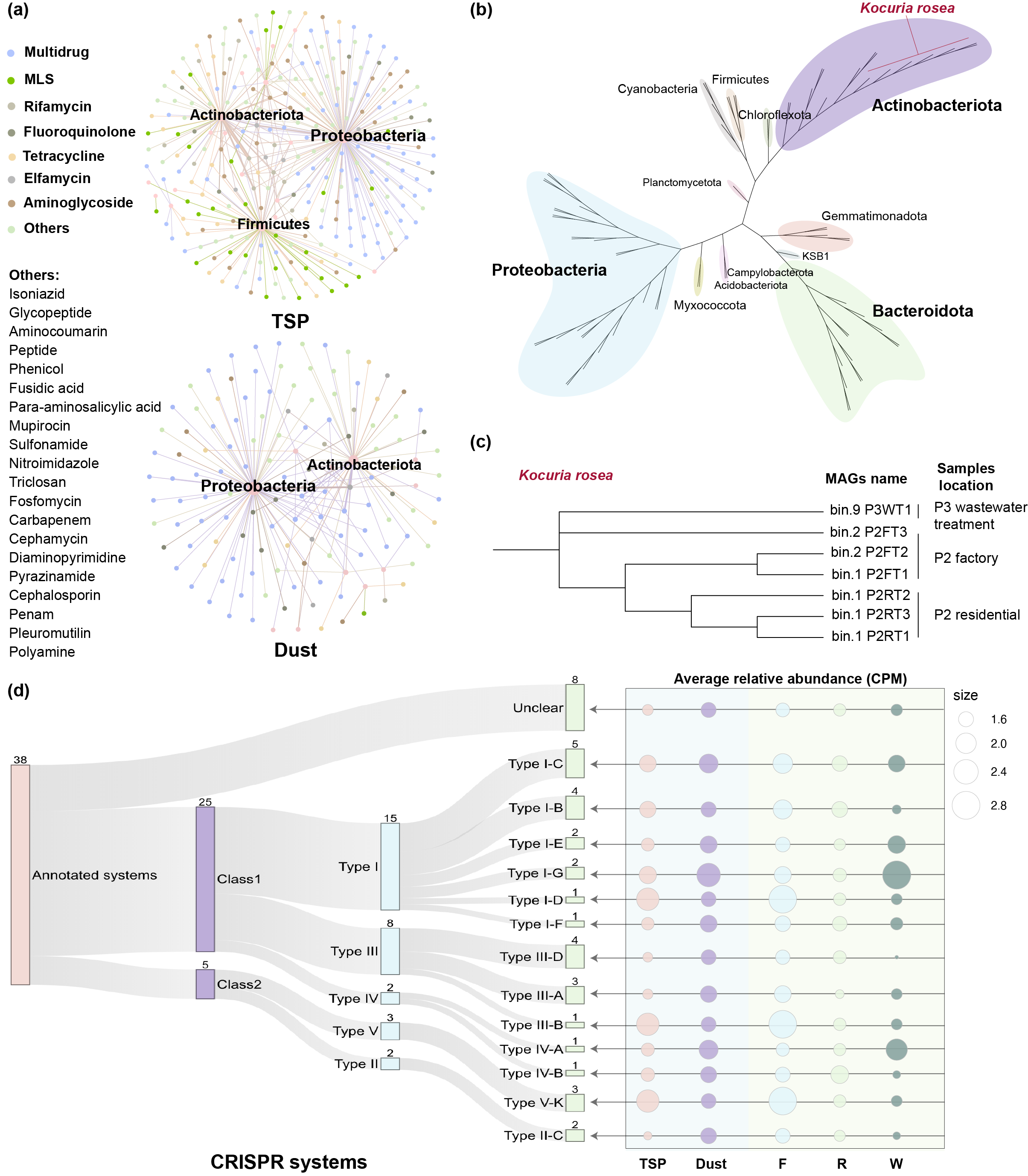
Figure 3. Hosts of airborne antibiotic resistance genes and CRISPR systems.
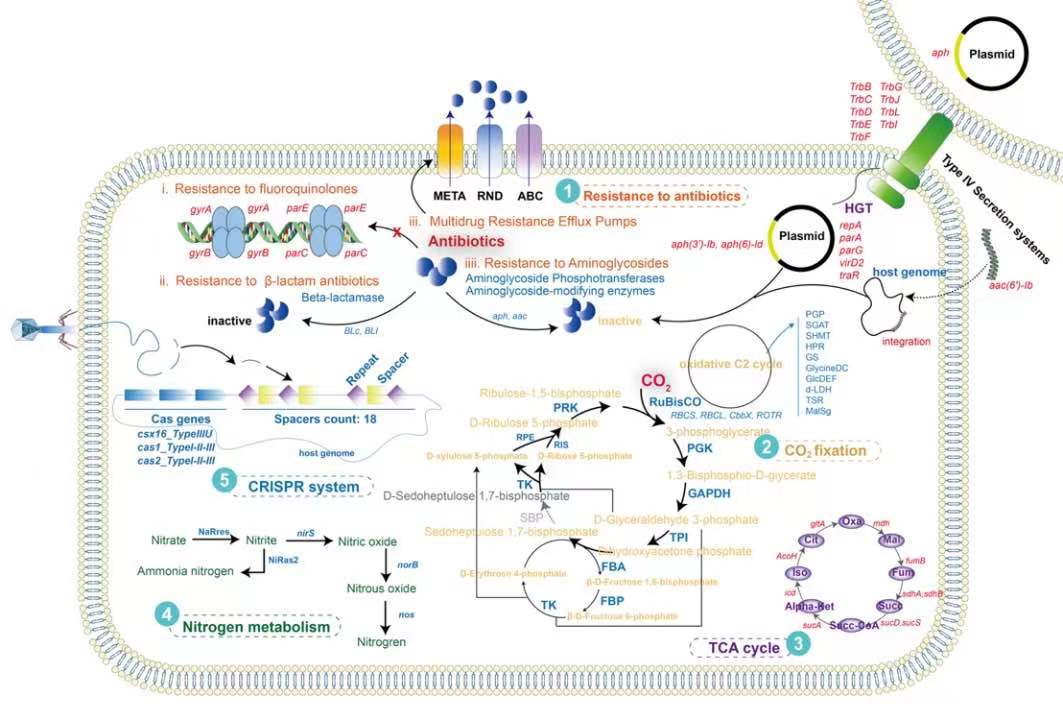
Figure 4. Overview of metabolic and antibiotic resistance potentials in bin.6_P3WA1.
宏基因组组装共获得80个高质量的宏基因组组装基因组(MAG),在这些MAG中,共注释到38个CRISPR阵列,主要类别为I-C、I-B和III-D型。此外,我们还注释了这些MAG的质粒和病毒序列中的ARGs。9个MAG中鉴定出质粒序列携带的ARG,仅在1个MAG中鉴定出病毒序列携带的ARG。制药厂气载ARG的潜在水平转移可能以质粒介导为主,但病毒在其中的作用也不容忽视。我们重点关注注释到最多ARG的MAG的胞内基础代谢和抗生素抗性功能。外排泵和抗生素裂解酶共同赋予该MAG的抗生素耐药性(多药、氟喹诺酮类、β-内酰胺和氨基糖苷类)。细胞膜上携带的蛋白质分泌系统(IV型分泌系统),能够通过水平转移获取外界ARG(aph),利用Plascad对aph(6)的接合质粒图谱进行了可视化。
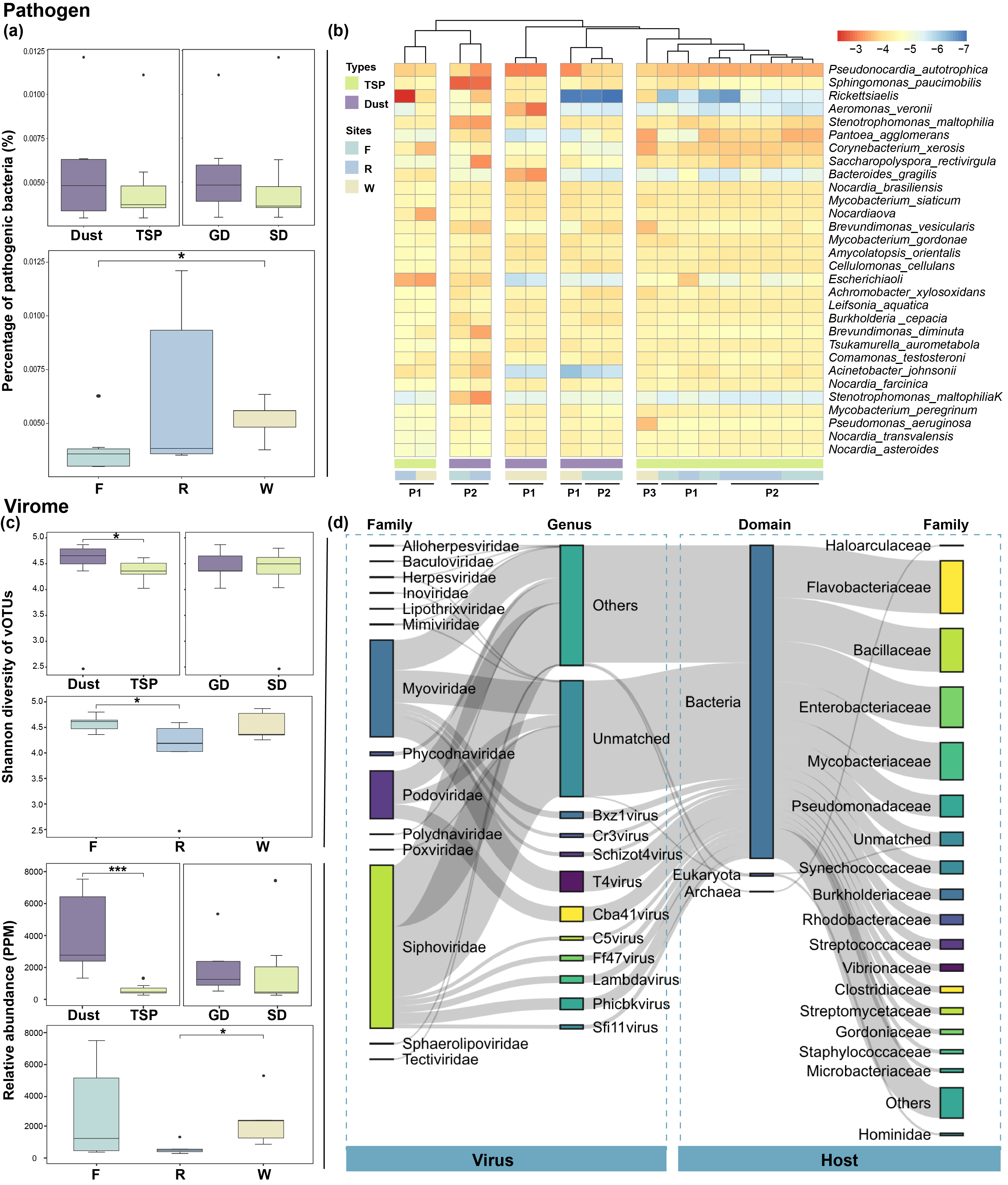
Figure 5. Profiles of airborne pathogens and virome in pharmaceutical factories.
为获取制药厂空气中病原微生物的分布特征,本研究从测序数据中提取了病原微生物的信息。研究显示污水处理区气载病原菌和噬菌体的相对丰度较高。总共鉴定了1,043个病毒操作分类单元(vOTU),其宿主包括细菌、真核生物和古细菌。进一步注释了由病毒组编码的ARGs,携带ARGs的病毒属于短尾噬菌体科、长尾噬菌体科和肌尾噬菌体科,值得强调的是,它们的宿主70%为人类关注的条件致病菌(如链球菌、分枝杆菌等)。

Figure 6. Airborne microbial risk and resistome risk.
研究筛选了制药厂空气高风险ARGs清单,其中27个ARGs被认为是制药厂中的高风险ARG(Risk I),14个ARGs被认为是核心高风险ARG(在所有药厂空气中均检出)。值得关注的耐药病原菌包括大肠埃希菌(Escherichia coli)、铜绿假单胞菌(Pseudomonas aeruginosa)、嗜水气单胞菌(Aeromonas hydrophila)、猪链球菌(Streptococcus suis)和肺炎链球菌(Streptococcus pneumoniae),携带aac(6)-I、aadE、ermT和tetM。
小结
本研究提供了制药厂空气抗生素抗性组和微生物组图谱。临床关注的ARGs和病原体在制药厂空气中广泛存在,气载ARGs的水平转移以质粒介导的转移为主,但噬菌体在其中的作用也不容忽视。制药厂的污水处理区是周边气载ARGs和ARB的主要来源。由于空气是一个动态生态系统,能够远距离传播并跨越地理障碍,因此其微生物组和抗性组与当地环境密切相关,考虑到空气中ARGs和ARBs的可传播性,与土壤和水相比,它对微生物生态系统的潜在环境影响范围可能更广。总体而言,这项研究证明了空气在ARGs传播过程中的关键作用,强调了制药厂附近工人和居民的潜在健康风险,并需要对空气中的高风险ARGs进一步研究。
致谢
本研究获得国家重点研发计划项目(2020YFC1806901)、国家自然科学基金(NSFC42030703,U22A20604和U1701242)、国家资助博士后研究人员计划(GZC20230870)的支持。
全文链接:https://doi.org/10.1016/j.envint.2024.108639